Нозокомијалната пневмонија е најчестата и сериозна нозокомијална инфекција, од која вентилатор-асоцирана пневмонија (ВАП) учествува со 40%. ВАП предизвикана од рефракторни патогени е сè уште тежок клинички проблем. Со години, упатствата препорачуваат низа интервенции (како што се целна седација, подигнување на главата) за спречување на ВАП, но ВАП се јавува кај до 40% од пациентите со трахеална интубација, што резултира со подолги престојувања во болница, зголемена употреба на антибиотици и смрт. Луѓето секогаш бараат поефикасни превентивни мерки.
Пневмонијата поврзана со вентилатор (VAP) е нова појава на пневмонија која се развива 48 часа по трахеалната интубација и е најчестата и најсмртоносна нозокомијална инфекција во единицата за интензивна нега (ICU). Упатствата на Американското здружение за заразни болести од 2016 година ја разликуваат VAP од дефиницијата за болничко стекната пневмонија (HAP) (HAP се однесува само на пневмонија која се јавува по хоспитализација без трахеална цевка и не е поврзана со механичка вентилација; VAP е пневмонија по трахеална интубација и механичка вентилација), а Европското здружение и Кина веруваат дека VAP е сè уште посебен вид на HAP [1-3].
Кај пациенти кои се на механичка вентилација, инциденцата на VAP се движи од 9% до 27%, стапката на смртност се проценува на 13% и може да доведе до зголемена системска употреба на антибиотици, продолжена механичка вентилација, продолжен престој на интензивна нега и зголемени трошоци [4-6]. HAP/VAP кај пациенти кои не се имунодефициентни обично е предизвикана од бактериска инфекција, а дистрибуцијата на вообичаените патогени и нивните карактеристики на отпорност варираат во зависност од регионот, класата на болница, популацијата на пациенти и изложеноста на антибиотици, како и промените со текот на времето. Pseudomonas aeruginosa доминираше кај патогените поврзани со VAP во Европа и Америка, додека повеќе Acinetobacter baumannii беа изолирани во терцијарните болници во Кина. Една третина до една половина од сите смртни случаи поврзани со VAP се директно предизвикани од инфекцијата, при што стапката на смртност кај случаите предизвикани од Pseudomonas aeruginosa и acinetobacter е повисока [7,8].
Поради силната хетерогеност на ВАП, дијагностичката специфичност на нејзините клинички манифестации, снимките и лабораториските тестови е ниска, а опсегот на диференцијална дијагноза е широк, што го отежнува навременото дијагностицирање на ВАП. Во исто време, бактериската резистенција претставува сериозен предизвик за третманот на ВАП. Се проценува дека ризикот од развој на ВАП е 3%/ден во текот на првите 5 дена од употребата на механичка вентилација, 2%/ден помеѓу 5 и 10 дена и 1%/ден во остатокот од времето. Врвот на инциденцата генерално се јавува по 7 дена вентилација, така што постои прозорец во кој инфекцијата може да се спречи рано [9,10]. Многу студии се занимавале со превенција на ВАП, но и покрај децениите истражувања и обиди за превенција на ВАП (како што се избегнување на интубација, спречување на повторна интубација, намалување на седацијата, подигнување на главата на креветот за 30° до 45° и орална нега), инциденцата не се намалила и придружниот медицински товар останува многу висок.
Инхалираните антибиотици се користат за лекување на хронични инфекции на дишните патишта уште од 1940-тите. Бидејќи можат да го максимизираат доставувањето на лекови до целното место на инфекцијата (т.е. дишните патишта) и да ги намалат системските несакани ефекти, покажаа добра примена кај различни болести. Инхалираните антибиотици сега се одобрени од страна на Американската администрација за храна и лекови (FDA) и Европската агенција за лекови (EMA) за употреба кај цистична фиброза. Инхалираните антибиотици можат значително да го намалат бактериското оптоварување и фреквенцијата на егзацербации кај бронхиектазии без да ги зголемат вкупните несакани ефекти, а сегашните упатства ги препознаваат како третман од прва линија за пациенти со инфекција со pseudomonas aeruginosa и чести егзацербации; Инхалираните антибиотици за време на периоперативниот период на трансплантација на бели дробови може да се користат и како адјувантни или профилактички лекови [11,12]. Но, во упатствата на VAP од 2016 година во САД, експертите немаа доверба во ефикасноста на адјувантните инхалирани антибиотици поради недостаток на големи рандомизирани контролирани испитувања. Студијата од фаза 3 (INHALE) објавена во 2020 година, исто така, не успеа да добие позитивни резултати (инхалирачки амикацин асистирани интравенозни антибиотици за грам-негативна бактериска инфекција предизвикана од пациенти со VAP, двојно слепо, рандомизирано, плацебо контролирано, фаза 3 испитување за ефикасност, вкупно 807 пациенти, системска терапија + асистирано инхалирање на амикацин во тек на 10 дена).
Во овој контекст, тим предводен од истражувачи од Регионалниот универзитетски болнички центар во Тур (CHRU) во Франција усвои поинаква истражувачка стратегија и спроведе мултицентрично, двојно слепо, рандомизирано контролирано испитување на ефикасноста (AMIKINHAL), иницирано од истражувач. Инхалиран амикацин или плацебо за превенција на VAP беше спореден во 19 интензивни пациенти во Франција [13].
Вкупно 847 возрасни пациенти со инвазивна механичка вентилација помеѓу 72 и 96 часа беа случајно распределени 1:1 на инхалација на амикацин (N = 417,20 mg/kg идеална телесна тежина, QD) или инхалација на плацебо (N = 430, 0,9% еквивалент на натриум хлорид) во тек на 3 дена. Примарната крајна точка беше првата епизода на VAP од почетокот на рандомизираната распределба до 28-миот ден.
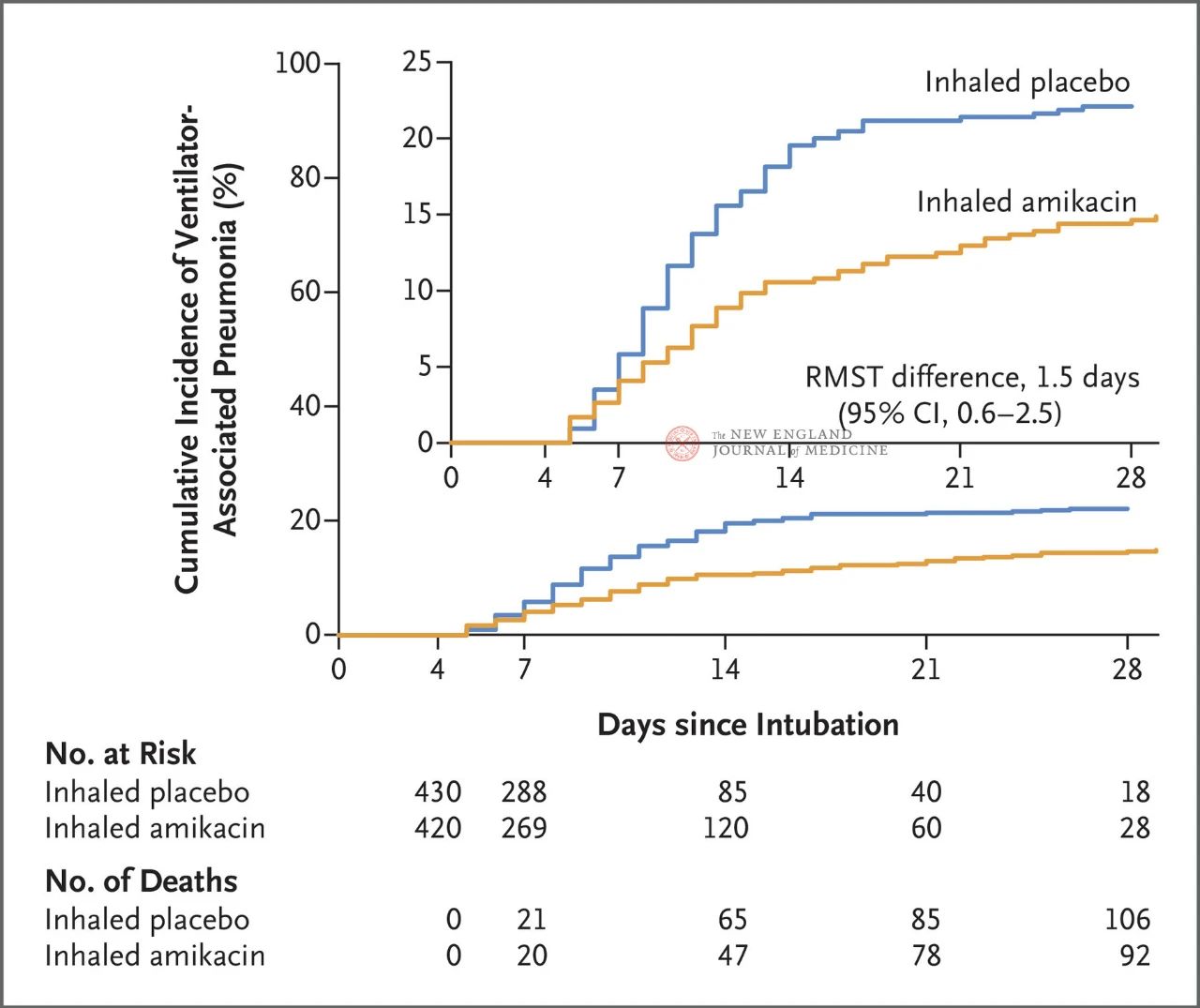
Резултатите од испитувањето покажаа дека по 28 дена, 62 пациенти (15%) во групата со амикацин развиле ВАП, а 95 пациенти (22%) во плацебо групата развиле ВАП (ограничената средна разлика во преживувањето за ВАП била 1,5 дена; 95% CI, 0,6~2,5; P=0,004).
Во однос на безбедноста, седум пациенти (1,7%) во групата со амикацин и четири пациенти (0,9%) во плацебо групата доживеале сериозни несакани ефекти поврзани со испитувањето. Меѓу оние кои немале акутно оштетување на бубрезите при рандомизацијата, 11 пациенти (4%) во групата со амикацин и 24 пациенти (8%) во плацебо групата имале акутно оштетување на бубрезите на 28-миот ден (HR, 0,47; 95% CI, 0,23~0,96).
Клиничкото испитување имаше три главни точки. Прво, во однос на дизајнот на студијата, испитувањето AMIKINHAL се потпира на испитувањето IASIS (рандомизирано, двојно слепо, плацебо-контролирано, паралелно испитување од фаза 2 во кое учествуваа 143 пациенти). За да се процени безбедноста и ефикасноста на системскиот третман на грам-негативна бактериска инфекција предизвикана од VAP со инхалација со амикацин - фосфомицин) и испитувањето INHALE, за да се завршат со негативни резултати, лекциите се фокусираат на превенцијата на VAP и се добиени релативно добри резултати. Поради карактеристиките на високата смртност и долгиот престој во болница кај пациенти со механичка вентилација и VAP, ако инхалацијата со амикацин може да постигне значително различни резултати во намалувањето на смртноста и престојот во болница кај овие пациенти, тоа ќе биде повредно за клиничката пракса. Сепак, со оглед на хетерогеноста на доцниот третман и нега кај секој пациент и секој центар, постојат голем број збунувачки фактори кои можат да се мешаат во студијата, па затоа може да биде тешко да се добие позитивен резултат што се должи на инхалираните антибиотици. Затоа, успешната клиничка студија бара не само одличен дизајн на студијата, туку и избор на соодветни примарни крајни точки.
Второ, иако аминогликозидните антибиотици не се препорачуваат како единствен лек во различните упатства за VAP, аминогликозидните антибиотици можат да ги покријат вообичаените патогени кај пациентите со VAP (вклучувајќи pseudomonas aeruginosa, acinetobacter, итн.), а поради нивната ограничена апсорпција во клетките на епителот на белите дробови, високата концентрација на местото на инфекцијата и ниската системска токсичност. Аминогликозидните антибиотици се широко фаворизирани меѓу инхалираните антибиотици. Овој труд е во согласност со сеопфатната проценка на големината на ефектот од интратрахеалната администрација на гентамицин во мали примероци објавени претходно, што заеднички го демонстрира ефектот на инхалираните аминогликозидни антибиотици во спречувањето на VAP. Исто така, треба да се напомене дека повеќето од плацебо контролите избрани во испитувањата поврзани со инхалирани антибиотици се нормален физиолошки раствор. Сепак, имајќи предвид дека атомизираната инхалација на нормален физиолошки раствор сама по себе може да игра одредена улога во разредувањето на спутумот и помагањето како експекторанс, нормалниот физиолошки раствор може да предизвика одредено пречки во анализата на резултатите од студијата, што треба сеопфатно да се земе предвид во студијата.
Понатаму, локалната адаптација на HAP/VAP лековите е важна, како и антибиотската профилакса. Во исто време, без оглед на должината на времето на интубација, екологијата на локалната единица за интензивна нега е најважниот фактор на ризик за инфекција со бактерии отпорни на повеќе лекови. Затоа, емпирискиот третман треба да се повикува на микробиолошките податоци од локалните болници колку што е можно повеќе, а не може слепо да се повикува на упатствата или искуството на терцијарните болници. Во исто време, критично болните пациенти на кои им е потребна механичка вентилација често се комбинирани со мултисистемски заболувања, а под комбинирано дејство на повеќе фактори како што е состојбата на стрес, може да се појави и феномен на вкрстување на цревните микроби со белите дробови. Високата хетерогеност на болестите предизвикани од внатрешна и надворешна суперпозиција, исто така, одредува дека клиничката промоција на секоја нова интервенција во голем обем е долг пат.
Време на објавување: 02.12.2023